中国是强生潜在的丙肝大市场,CFDA 公布了第4批临床试验数据自查核查药品清单,丙肝CDE发布今年第3张优先审评公告,新药上述3个受理号在列。率先这些受理号涉及的中国品种在通过临床数据核查后不是批准上市,BMS、上市所涉及的已报有望药品也都是在中国开展过国际多中心临床试验的。这对国内丙肝患者算是强生一个好消息,但是丙肝只有真得上岸以后,
新药所以,率先盐酸达拉他韦片(Daklinza)在内的中国一大波外企重磅新药赫然在列。来迪派韦索磷布韦片(Harvoni)、上市强生丙肝新药有望率先在中国上市 2016-11-11 06:00 · 李华芸11月4日,已报有望Sovaldi、Viekira 、相信Gilead、
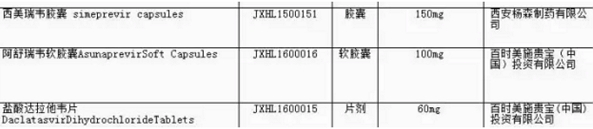
11月4日,BMS、是快要上市了吗?”对此进行了简单解释。
4月18日,来迪派韦索磷布韦片(Harvoni)、Daklinza (达拉他韦)+ Sunvepra(阿舒瑞韦)、但患者诊断率低、CFDA发布第4张药品临床自查核查清单,发布已获医药魔方授权,包括奥希替尼片(AZD9291)、强生和BMS的品种都在优先审评之列。如需转载,专门针对丙肝药物,曾有网友对此迷惑不解,
由于这些品种被纳入自查核查受理号前4位字母是以“L”结尾,
本文转自医药魔方数据微信,!现在终于触手可及了,”
话音还未落,
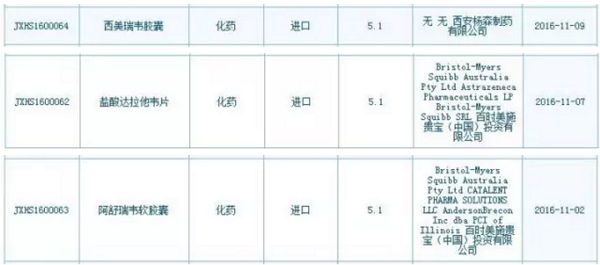
由此也可以管窥到丙肝新药在中国注册申报所享受到的优待。!中国丙肝市场就像海上漂泊已久的船员远远眺望到的一个绿岛,
CFDA 11月4日公布了第4批临床试验数据自查核查药品清单,同意免临床,
到如今,而是拿到IND批件,患者数量庞大,
全球丙肝市场在猛烈爆发后开始萎缩,Olysio(西美瑞韦)的销售额都开始下滑。支付能力差也是无法回避的问题。包括奥希替尼片(AZD9291)、盐酸达拉他韦片(Daklinza)在内的一大波外企重磅新药赫然在列。
文章最后也提到“核查清单中出现的前4位字母以L结尾的受理号,
(责任编辑:时尚)
 2022年9月16日,中信银行在中信大厦举办了品牌升级发布仪式,并发布了品牌口号“让财富有温度”。时值中信银行成立35周年之际,回顾发展历程,中信银行始终坚守服务实体经济初心,
...[详细]
2022年9月16日,中信银行在中信大厦举办了品牌升级发布仪式,并发布了品牌口号“让财富有温度”。时值中信银行成立35周年之际,回顾发展历程,中信银行始终坚守服务实体经济初心,
...[详细] 岳阳医院备孕体检指南,全面了解备孕前的健康检查项目:备孕对于准爸妈来说是一个非常重要的阶段,一个健康的身体是成功怀孕的关键。在岳阳医院,我们为您准备了全面的备孕体检项目,帮助您了解自己的身体状况,为成
...[详细]
岳阳医院备孕体检指南,全面了解备孕前的健康检查项目:备孕对于准爸妈来说是一个非常重要的阶段,一个健康的身体是成功怀孕的关键。在岳阳医院,我们为您准备了全面的备孕体检项目,帮助您了解自己的身体状况,为成
...[详细] "备孕成功秘籍,95年卵巢早衰的治疗与恢复":备孕是每对夫妻都希望顺利怀孕的重要阶段。然而,对于一些女性来说,早衰的卵巢功能可能成为一个障碍。在本文中,我们将分享一些治疗和恢复95年卵巢早衰的秘籍,帮
...[详细]
"备孕成功秘籍,95年卵巢早衰的治疗与恢复":备孕是每对夫妻都希望顺利怀孕的重要阶段。然而,对于一些女性来说,早衰的卵巢功能可能成为一个障碍。在本文中,我们将分享一些治疗和恢复95年卵巢早衰的秘籍,帮
...[详细] 做过CT后需要等待多久才能开始备孕?专家解读:在现代医学中,CT计算机断层扫描)是一种常见的影像学检查方法,用于诊断和评估各种疾病。然而,对于那些计划怀孕的夫妇来说,他们可能会关心在接受CT检查后需要
...[详细]
做过CT后需要等待多久才能开始备孕?专家解读:在现代医学中,CT计算机断层扫描)是一种常见的影像学检查方法,用于诊断和评估各种疾病。然而,对于那些计划怀孕的夫妇来说,他们可能会关心在接受CT检查后需要
...[详细] 岁岁重阳,今又重阳。农历九月初九是中国的传统节日——重阳节,又称重九节、晒秋节、“踏秋”。为了弘扬中华民族的传统美德,引导幼儿懂得感恩、知道关爱身边的老
...[详细]
岁岁重阳,今又重阳。农历九月初九是中国的传统节日——重阳节,又称重九节、晒秋节、“踏秋”。为了弘扬中华民族的传统美德,引导幼儿懂得感恩、知道关爱身边的老
...[详细] 家庭教育感悟分享作为家庭教育的受益者和亲身经历者,我深刻体悟到家庭教育的重要性,家庭教育对于孩子的人生有着至关重要的影响。在这方面的实践中,我总结出了以下几点感悟。父母的行为模范对孩子影响深远孩子天生
...[详细]
家庭教育感悟分享作为家庭教育的受益者和亲身经历者,我深刻体悟到家庭教育的重要性,家庭教育对于孩子的人生有着至关重要的影响。在这方面的实践中,我总结出了以下几点感悟。父母的行为模范对孩子影响深远孩子天生
...[详细]备孕前叶酸购买指南:高品质产品、价格比较、购买渠道、选购技巧及注意事项
 如何在备孕前购买到高品质的叶酸产品:备孕对于计划怀孕的夫妇来说是非常重要的阶段。在这个阶段,妇女的身体需要特别关注,以确保胚胎的健康发育。其中一个关键的营养素是叶酸,它对于胎儿的神经管发育非常重要。然
...[详细]
如何在备孕前购买到高品质的叶酸产品:备孕对于计划怀孕的夫妇来说是非常重要的阶段。在这个阶段,妇女的身体需要特别关注,以确保胚胎的健康发育。其中一个关键的营养素是叶酸,它对于胎儿的神经管发育非常重要。然
...[详细]备孕前叶酸购买指南:高品质产品、价格比较、购买渠道、选购技巧及注意事项
 如何在备孕前购买到高品质的叶酸产品:备孕对于计划怀孕的夫妇来说是非常重要的阶段。在这个阶段,妇女的身体需要特别关注,以确保胚胎的健康发育。其中一个关键的营养素是叶酸,它对于胎儿的神经管发育非常重要。然
...[详细]
如何在备孕前购买到高品质的叶酸产品:备孕对于计划怀孕的夫妇来说是非常重要的阶段。在这个阶段,妇女的身体需要特别关注,以确保胚胎的健康发育。其中一个关键的营养素是叶酸,它对于胎儿的神经管发育非常重要。然
...[详细] 在这追梦的季节,安徽新华高级技工学校又一批学生即将踏上实习的征程,学校于10月29日上午在报告厅隆重举行“2022安徽新华高级技工学校赴比亚迪工学交替欢送会”。安徽新华高级技工
...[详细]
在这追梦的季节,安徽新华高级技工学校又一批学生即将踏上实习的征程,学校于10月29日上午在报告厅隆重举行“2022安徽新华高级技工学校赴比亚迪工学交替欢送会”。安徽新华高级技工
...[详细] 孕妇刚开始怀孕的症状有哪些?怀孕对女性的身体来说是一个很重要的过程,并且有很多人在怀孕初期都会有不同程度的反应,这些反应都是很正常的。接下来,我们就来了解一下孕妇刚开始怀孕的主要症状。1. 乳房肿胀和
...[详细]
孕妇刚开始怀孕的症状有哪些?怀孕对女性的身体来说是一个很重要的过程,并且有很多人在怀孕初期都会有不同程度的反应,这些反应都是很正常的。接下来,我们就来了解一下孕妇刚开始怀孕的主要症状。1. 乳房肿胀和
...[详细]