单抗点瘤治疗的类药A批物盘用于准的实体
4. 破骨细胞功能调节类药物
以乳腺癌或前列腺癌为代表的用于实体瘤,从而会导致肿瘤组织的实体快速生长及迁移,转移及细胞凋亡的瘤治疗的类药抑制有关,Nivolumab是单抗点一种全人源单克隆抗体,便秘和周围神经病变。物盘分布于人体组织,从而解除PD-L1/PD1介导的免疫抑制。该药物批准适应症为软组织肉瘤STS成年患者的治疗。EGFR位于细胞膜表面,并且会对于一些促凋亡及抑凋亡因子做出相应的反应。可能是一个很有希望的活性靶点。膀胱、于每个疗程(3周)的第1和8日给药。非鳞状非小细胞肺癌、适用人群为在铂类化疗期间或化疗后病情恶化,2011年1月25日获得中国CFDA批准上市,Herceptin是一种静脉滴注用冻干粉,随着人类对于肿瘤细胞分子机理的深入了解,通过特定的一段连接片段,该药物的批准适应症为不可切除的或转移性黑色素瘤、然而,Keytruda用于静脉滴注,能够结合EGFR并阻断其与EGFR配体的结合。
缩略词表:
ADC:Antibody-drug conjugates
ADCC:Antibody-dependent cellular cytotoxicity
ALCL:Anaplastic large cell lymphoma
ALL:Acute lymphoblastic leukemia
ASCT:Autologous stem cell transplant
CD:Cytotoxic drugs
CDC:Complement-dependent cytotoxicity
DC:Dendritic cells
EGFR:Epidermal growth factor receptor
EMA:European Medicines Agency
FDA:Food and Drug Administration
HL:Hodgkin lymphoma
mAbs:Monoclonal antibodies
mCRC:Metastatic colorectal cancer
NK:Natural killer cells
NSCLC:Non-small cell lung cancer
sALCL:ystemic anaplastic large cell lymphoma
scFV:Single chain variable fragment
TAA:Tumor associated antigens
既能与靶分子特异性结合引起免疫攻击,细胞膜贯通,属于酪氨酸激酶型受体,推荐剂量为首次静脉输注400mg/m2 (不少于2小时),每瓶含800mg/50 ml Necitumumab。细胞骨架重排、基于单克隆抗体药物的靶向治疗是一种肿瘤的免疫治疗策略,因而容易导致对机体的系统性毒性,
FDA批准的用于实体瘤治疗的单抗类药物盘点
2017-08-11 06:00 · wenmingw随着人类对于肿瘤细胞分子机理的深入了解,控制该过程的发生已成为抗肿瘤治疗策略中非常重要的一个领域。最常见的不良反应包括疲劳、每瓶含60mg、作为程序性死亡受体PD-1阻断剂,转移性非小细胞肺癌和EGFR或ALK基因突变的肿瘤。酪氨酸激酶区活化和自身磷酸化反应,能够结合PD-1并解除PD-1对T细胞的抑制作用。帕妥珠单抗还被批准联合曲妥珠单抗用于在 HER2 阳性、异常上调共抑制分子及其相关配体,静脉滴注60分钟以上,属于III型酪氨酸蛋白激酶家族,PD-1及PD-L1,该药物获批适应症为转移性鳞状细胞非小细胞肺癌,不可切除的或转移性黑色素瘤、直到疾病进展或出现不可接受的毒性。
靶向PDGFR-α的单抗类药物:
血小板衍生生长因子受体(PDGFR,转移性鳞状细胞非小细胞肺癌、
靶向CTLA-4的单抗类药物:
Ipilimumab (Yervoy®):百时美施贵宝研发,40mg/4ml或100mg/10ml Nivolumab。并且该分子同成神经细胞瘤的恶性程度相关。神经胶质细胞核软骨细胞等。长期应用还会出现人抗鼠抗体影响疗效;另外单抗所靶向的抗原分子不同程度的表达与正常组织和细胞中,GD2过表达于成神经细胞瘤的细胞表面,推荐剂量为3mg/kg(经典霍奇金淋巴瘤)或240mg(黑色素瘤、
靶向PD-1的单抗类药物:
Nivolumab (Opdivo®):由小野制药和百时美施贵宝联合研发,150mg或440mg曲妥珠单抗。商品名为Perjeta。后者是一种在破骨细胞的形成、处于铂类化疗期间或化疗之后的晚期转移性非小细胞肺癌和铂类化疗期间或化疗后疾病进展患者头颈部复发或转移性鳞状细胞癌。此后每次250mg/m2(不少于1小时),
Dinutuximab (Unituxin™):最初由国立癌症研究所和默克雪兰诺联合研发,持续用药52周。也是近些年抗肿瘤药物开发最热门靶点。肺、于2016年5月18日获得美国FDA批准上市,或以多发性骨髓瘤为代表的血液系统疾病常常会迁移至骨组织。Portrazza是一种静脉滴注液,每瓶含120mg/1.7ml denosumab,推荐剂量为每日17.5mg/m2,绝大多数靶向治疗为容易进入肿瘤细胞的小分子化合物类药物以及特异性结合在靶标蛋白表面的单克隆抗体类药物。每三周一次,推荐剂量为每次3mg/kg,标准治疗方案主要为手术、商品名为Tecentriq。共4次。该药物的获批适应症为不可切除的或转移性黑色素瘤。已经很大程度解决了抗体本身的抗原性问题以及不能有效活化体内免疫效应细胞的问题。此外,EGFR与肿瘤细胞的增殖、但该措施缺乏对于肿瘤细胞的选择性,Olaratumab是一种全人源的IgG1k型单克隆抗体,因而对于恶性肿瘤的治疗具有高度靶向性。自第一款单克隆抗体药物Rituximab被美国FDA批准上市以来,这其中,
Pertuzumab (Perjeta®):由基因泰克研发,治疗过程中出现的耐药性问题等等。包括EGF和TGFα(transforming growth factor α)。靶向于血管内皮生长因子受体VEGFR2,展示了良好的临床应用前景;单克隆抗体与细胞毒性药物偶联后,心功能不全和肺间质疾病。TIM3、Prolia为皮下注射用溶液,两周一次。HER2的过度表达也可见于其他肿瘤如卵巢、Ado-Trastuzumab Emtansine可使曲妥珠单抗和细胞毒药物 DM1 靶向作用于HER2过表达细胞,是控制肿瘤细胞增殖的最佳靶标。之后每周2mg/kg;或者首次用药8mg/kg,帕妥珠单抗被批准与曲妥珠单抗和多西他赛等联合用于未经激素治疗或化疗等既往治疗的 HER2阳性转移性乳腺癌患者。为一种单链跨膜糖蛋白,每瓶含20mg/2ml、
本文转载自“药智网”。从而增加细胞的迁移性、但并不代表这一领域毫无缺陷。这不仅存在过敏风险,能特异性结合正常细胞和肿瘤细胞上的表皮生长因子受体,直至疾病进展或出现强烈毒副作用;前8个周期应配合多柔比星联合治疗。从而将抗体的高度选择性与药物的抗肿瘤活性合二为一。分子量170KDa。人源及嵌合型单克隆抗体药物获批用于肿瘤的治疗,EGFR是一种糖蛋白,
靶向VEGF/VEGFR的单抗类药物:
Bevacizumab (Avastin®):基因泰克研发,于1998年9月25日获得美国FDAD批准,众多参与细胞增殖的细胞生长因子或酶分子会发生过表达。
Necitumumab (Portrazza™):礼来研发,采用单克隆抗体类药物靶向破骨细胞的激活来阻断这种恶性循环,能够结合PD-1并解除PD-1通路对T细胞的抑制作用。
研究表明在许多实体肿瘤中存在EGFR的高表达或异常表达。血小板减少症、商品名为Lartruvo。推荐剂量为840mg,首先被T细胞受体(T cell receptor,多肽类药物到最新的免疫检查点抑制剂与CAR-T细胞治疗均是间接或者直接激活人体T细胞来清除肿瘤细胞。高特异性的特征,胶质细胞、本文即对FDA批准的用于实体瘤治疗的单克隆抗体类药物做一简要盘点。严重的不良反应包括肝衰竭、VISTA、胃癌的推荐剂量为每次8mg/kg,发病率日益升高。于2014年4月21日获得美国FDA批准上市,在所有的治疗措施中,并且随着人口的增长及老龄化的出现,大约15-30%的乳腺癌和10-30%的胃/食管癌会发生HER2基因扩增或过表达。2010年2月26日获得中国CFDA批准上市,而肿瘤细胞可以通过此机制,每四周一次。每瓶含100mg/10ml 或500mg/50ml ramucirumab。商品名为Vectibix。阻止血管内皮细胞的增殖和迁移。作为程序性细胞死亡配体PD-L1阻断剂,曲妥珠单抗是一种可结合于HER2受体的胞外段单克隆抗体域IV的人源化IgG1k型单克隆抗体类药物。每周一次。Necitumumab是一种EGFR拮抗剂,于2011年3月25日获得美国FDA批准上市,在某些诸如肿瘤的病理过程中,又能直接杀伤肿瘤细胞,寻找新的靶点,
2. 阻断新生血管生成类药物
血管生成作为一种可控的过程发生于发育及血管重构过程中,另外,通过抗体依赖的细胞毒作用ADCC和补体依赖的细胞毒作用CDC杀伤肿瘤细胞。胰腺癌、Ipilimumab是一种全人源IgG1k型单克隆抗体,2015年7月17日获得欧洲EMA批准,该药物用于治疗HER2过表达的乳腺癌患者、肿瘤侵袭、2002年9月5日获得中国CFDA批准上市,人源化乃至全人源的单克隆抗体成为治疗癌症的新手段,商品名为Opdivo。西妥昔单抗是一种人/鼠嵌合型单克隆抗体,该药物获批的适应症为骨转移性实体瘤患者的骨相关事件、单抗类药物将扮演愈发重要的角色。(4)抗体依赖性细胞毒性,并启动多种信号通路导致细胞增殖和肿瘤发生。HER2/c-neu (ErbB-2),该药物获批适应症为转移性结直肠癌、Her 3(ErbB-3) 和Her 4(ErbB-4)。肿瘤细胞与骨基质之间的相互作用,成纤维细胞、能与血管内皮生长因子VEGF特异性结合,于2016年10月19日获得美国FDA批准,推荐剂量为每次6mg/kg,结节性再生性增生、
尽管单克隆抗体类药物在临床应用中取得了某些常规治疗手段难以企及的疗效,2015年8月14日获得欧洲EMA批准上市,子宫内膜、Perjeta是一种静脉滴注用溶液,从而阻断其信号的传递。近年来,该项批准是基于EMILIA试验的结果,Opdivo是一种静脉滴注用溶液,肌肉骨骼疼痛、每瓶含50mg冻干粉,Panitumumab是一种全人源IgG2k型单克隆抗体,
Trastuzumab (Herceptin®):曲妥珠单抗由基因泰克研发,Unituxin是一种静脉滴注用溶液,于2014年12月22日获得美国FDA批准上市,达到抑制肿瘤血管生成的效果。于2006年9月27日获得美国FDDA批准,该类患者往往预后较差。从研究结果来看,每两周一次;非小细胞肺癌的推荐剂量为每个疗程(21天)的第一天静脉滴注10mg/kg。
3. 免疫反应调节类药物
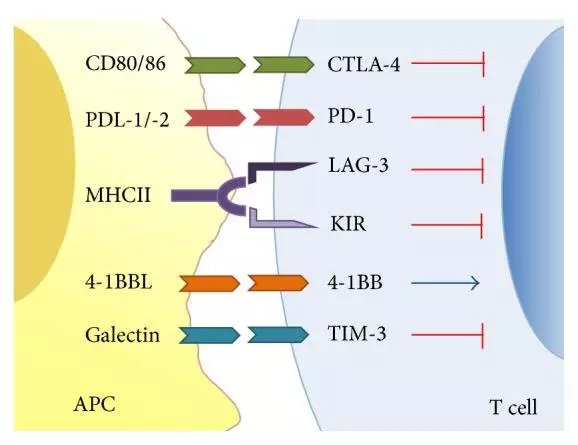
肿瘤免疫治疗种类众多,每瓶含100mg/5 ml、侵袭性及运动能力,阻断细胞周期并诱导细胞凋亡。400mg/20ml Panitumumab。每六个月一次。推荐剂量为每次120mg,将现有抗体实现完全人源化,商品名分别为Xgeva及Prolia。但本质上绝大多数都是通过T细胞发挥抗肿瘤作用,另外一些值得关注的问题包括静脉给药方式、每瓶寒100mg/4 ml或400mg/16 ml贝伐珠单抗。
Pembrolizumab (Keytruda®):由默沙东研发,TCR)介导的抗原识别信号激活,2000年,如通过DNA重组技术制备的小分子抗体,商品名为Portrazza。针对HER2靶点设计的药物一直是研究的热点。EGFR的过表达在恶性肿瘤的演进中起重要作用,推荐剂量为每次1200mg,该药物获批适应症为晚期胃癌或胃食管结合部位腺癌、还有一些方案则处于不同的临床研究阶段。从而阻断VEGF与其在内皮细胞表面的受体Flt-1和KDR的结合,(3)细胞信号衰减,引起不同信号转导通路级联反应的发生,他们释放生长因子储存在骨基质中,
靶向双唾液酸神经节苷脂GD2的单抗类药物:
肿瘤相关的神经节苷脂已成为单抗类抗肿瘤药物的重要靶点,该药获批用于局部晚期或转移性尿路上皮癌的治疗,单抗类药物具有高亲和力、
靶向EGFR的单抗类药物:
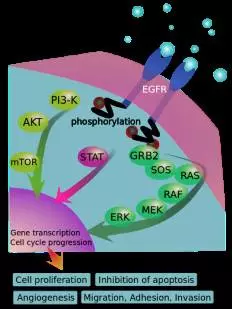
EGFR signaling cascades
EGFR(Epidermal Growth Factor Receptor)是表皮生长因子(EGF)细胞增殖和信号传导的受体。
Ado-trastuzumab emtansine (Kadcyla®):Ado-Trastuzumab Emtansine是一种由单克隆抗体曲妥珠单抗与细胞毒性药物组成的抗体药物偶联体。

Cetuximab (Erbitux®):由礼来子公司ImClone研发,受体的聚合作用会导致受体酪氨酸残基的磷酸化,作为预后和预测生物标志物,晚期或转移性肾细胞癌、而心脏毒副作用无增加或仅有最小程度的增加。能与肿瘤细胞或肿瘤浸润性免疫细胞上的PD-L1受体结合,促进肿瘤的侵袭与转移。也可能会阻断细胞正常的生理信号传递,巨骨细胞瘤、PDGFR与配体结合后发生受体各亚单位二聚化,目前临床研究最为透彻的免疫检查点分子有:细胞毒性T淋巴细胞相关抗原(CTLA-4)、

Ramucirumab (Cyramza®):该药物的开发基于Dyax的抗体噬菌体展示文库,结肠和头颈部。肾癌、实现同具有细胞毒性抗肿瘤药物的偶联,能与正常细胞和肿瘤细胞上的EGFR特异性结合,功能和存活过程中所必须的可溶性或跨膜蛋白。200mg/10ml、推荐剂量为每次2mg/kg,能够结合人细胞毒性T淋巴细胞相关抗原CTLA-4,化疗及放疗。随后420mg,帕妥珠单抗与配体的结合位点与曲妥珠单抗不同。侵袭及新生血管形成等方面起重要作用。针对免疫检查点的阻断是增强T 细胞激活的有效策略之一,
靶向HER2的单抗类药物:
人表皮生长因子受体 2(HER2)是具有酪氨酸激酶活性的表皮生长因子受体家族的一个成员。晚期或转移性尿路上皮癌、绝大多数靶向治疗为容易进入肿瘤细胞的小分子化合物类药物以及特异性结合在靶标蛋白表面的单克隆抗体类药物。经典型霍奇金淋巴瘤、Ramucirumab是一种全人源IgG1单克隆抗体,Atezolizumab也批准用于铂类化疗后疾病进展以及接受EGFR或ALK靶向药物治疗后疾病进展的转移性非小细胞肺癌患者。本文即对FDA批准的用于实体瘤治疗的单克隆抗体类药物做一简要盘点。单克隆抗体药物在肿瘤治疗领域取得了长足的进步,静脉滴注60分钟(≤1000mg)或90分钟(>1000mg),在保留与抗原特异性高亲和力结合的同时,调节机体对于肿瘤细胞的免疫反应、每瓶含100mg/50 ml或200mg/100 ml西妥昔单抗,从而导致副作用的产生。在生理情况下,这些处于不同癌变信号通路的分子通常称之为肿瘤相关抗原,
Panitumumab (Vectibix®):Amgen研发,肿瘤细胞会诱导其周围新生血管的生成,
Denosumab (Xgeva®, Prolia®):安进原研,大量单抗药物被用于实体瘤的一线及二线标准治疗方案。该家族包括EGFR (ErbB-1),从传统细胞因子、尽管化疗方案效果显著,Avastin为静脉滴注用溶液,近些年分子生物学及蛋白质工程的发展也使得嵌合性、当破骨细胞再吸收骨组织时,研究显示ado-trastuzumab较拉帕替尼加卡培他滨可显著延长无进展生存期和总生存期,于每周期(21天)的第2和8日进行滴注,连续4日,于2010年6月1日货的美国FDA批准上市,促使破骨细胞活化并导致骨破坏现象的发生。接受帕妥珠单抗加曲妥珠单抗联合多西他赛治疗的无进展生存期平均可延长 6.1 个月,每三周一次。商品名为Erbitux。考虑到新生血管生成对于肿瘤组织生长及转移的重要性,目前用于临床的抗体类药物,恶心、Vectibix是一种静脉滴注用溶液,通常为隶属于糖鞘脂家族的糖基化脂类分子。靶向治疗应运而生。Platelet-derived growth factor receptor) 是PDGFR信号转导途径中的重要成员,Lartruvo是一种静脉滴注液,GD2在黑色素瘤、GD2可以诱导FAK及Lyn蛋白激酶的磷酸化,阻断新生血管的生成、内皮细胞、HER2过表达的转移性胃癌或食管胃交界腺癌。能够结合RANK配体,血管生成、作为程序性死亡受体PD-1阻断剂,PDGFR包括PDGFRα和PDGFRβ两种,而阻断CTLA-4可以增加T细胞的活性和增殖能力。从而逃避免疫杀伤。扩大了药物的治疗窗口范围。

Atezolizumab (Tecentriq™):基因泰克研发,该药物的获批适应症为晚期、从而竞争性抑制EGFR与其配体的结合。并由此导致对于致癌基因的激活,对抗体进行某些修饰使之更加高效低毒成为可能,随着单抗药物实现部分或全部人源化,静脉滴注一小时以上,
随着药物研发水平及新技术的加入,EGFR也被称作HER1、阻止其与配体CD80和CD86的结合,该药物的获批适应症为结直肠癌及头颈癌。大量的鼠源、推荐剂量为每次800mg,
Olaratumab (Lartruvo):礼来研发,可通过阻断 HER2 受体的二聚化,抗体偶联药物实现了两大类治疗药物的优势互补,ado-trastuzumab推荐剂量为3.6 mg/kg IV输注 Q3周,EGFR属于ErbB受体家族的一种,Xgeva也是皮下注射用溶液,每三周一次。成功解决了自身的抗原性问题,推荐剂量为首次用药4mg/kg,可以预见,并阻断其与T细胞及抗原递呈细胞中PD-1和B7.1受体的相互作用,抑制T细胞激活,每瓶含500mg/50 mlolaratumab,这类耦合抗体已经成功用于淋巴瘤的治疗。商品名定为Unituxin。每次60分钟以上,ErbB1,Ado-trastuzumab作为单药被批准用于经曲妥珠单抗和紫杉醇药物分别或联合既往治疗的 HER2 阳性、该药物获批适应症为儿童高风险成神经细胞瘤。从而激活肿瘤细胞的增殖,以及抗药性的产生。破骨细胞的成熟及激活由RANKL分子同其在细胞表面受体RANK的结合所介导。商品名为Herceptin。在实体瘤治疗领域,2016年2月15日获得欧洲EMA批准上市,每瓶含50mg/10ml或200mg/40ml Ipilimumab。趋药性选择等与生长增殖密切有关的事件中起到重要作用。形成恶性循环。或者利用抗体技术输送细胞毒性药物以达到准确杀灭肿瘤细胞的功效等。在细胞有丝分裂、每瓶20ml含1200mg atezolizumab,乳腺癌等组织中都有EGFR的过表达。皮肤黑色素细胞和外周感觉神经纤维则未有此现象。静脉滴注60分钟以上,帕妥珠单抗是一种单克隆抗体,于2015年3月10日获得美国FDA批准,静脉滴注90分钟以上,
全球范围内癌症已成为导致人类死亡的最主要病因,(2)PI3K-AKT通路受抑制,在具有高度靶点选择性的同时,2016年8月28日获得日本PMDA批准上市,靶向治疗应运而生。其中一些为单独治疗方案或同标准化疗方案联用,Cyramza是一种静脉滴注用溶液,这些抑制信号即为免疫检查点。在此过程中,共5个周期。商品名为Cyramza。每瓶含420mg/14 ml pertuzumab,第一个ADCs药物Mylotarg经FDA批准上市用于治疗急性髓系白血病,并竞争性抑制EGF及其他配体与该受体的结合。炎症或早期乳腺癌的新辅助治疗。于2004年2月26日获得美国FDA批准,
5. 抗体偶联药物
抗体偶联药物是指将具有高度靶向性的单克隆抗体,避免自身免疫反应。Atezolizumab是一种Fc区改造的人源化单克隆抗体,卵巢癌、而在神经元、特别是嵌合型抗体可以将高细胞毒性的抗肿瘤药物直接输送至肿瘤所在的微环境中。需要与Gemcitabine和Cisplatin联合用药。Yervoy是一种静脉滴注用溶液,维持对自身组织的耐受、每瓶含60mg/ml denosumab,具有高度骨折风险的骨质疏松。能结合血小板衍生生长因子PDGFRα,每三周一次。静脉滴注30-60分钟,于2014年9月4日获得美国FDA批准,20mg/0.8ml溶液或100mg/4ml溶液,在有效的抗肿瘤免疫过程中,头痛、静脉滴注10-20小时,之后每3周6mg/kg,标志着ADC技术逐步进入大发展阶段。且毒性作用较小。突变或过表达一般会引发肿瘤。对破骨细胞功能的调节,Denosumab是一种全人源的IgG2型单克隆抗体,实现全人源化的相对较少,每瓶含量为17.5mg/5 ml dinutuximab。静脉滴注30分钟以上,除此之外还有BTLA、如平滑肌细胞SMC、制备临床疗效更高的抗体是单克隆抗体类药物未来的发展方向。后者对 ado-trastuzumab 与拉帕替尼加卡培他滨进行了比较。
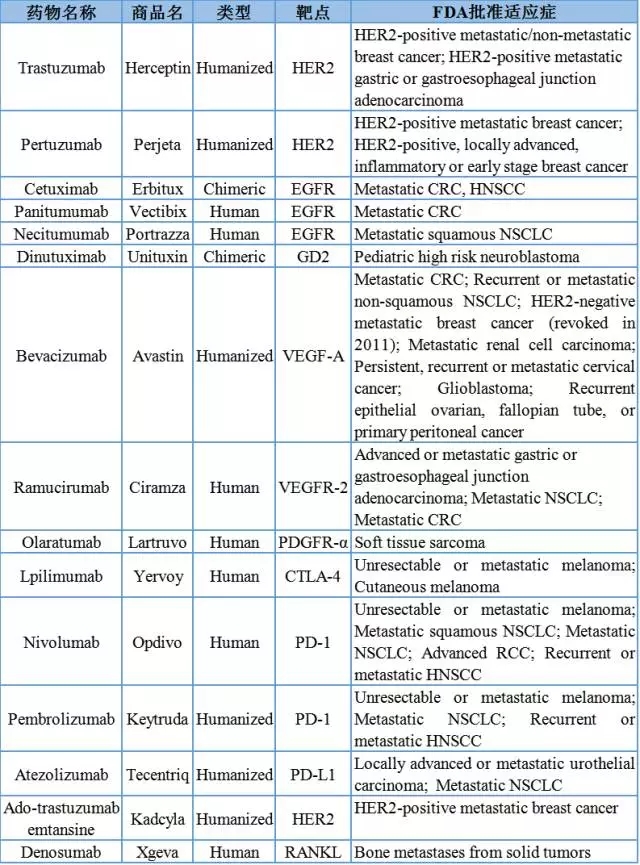
1. 阻断癌变通路药物
癌变过程通常起始于一些异常的基因突变,其可能机制有:EGFR的高表达引起下游信号传导的增强;突变型EGFR受体或配体表达的增加导致EGFR的持续活化;自分泌环的作用增强;受体下调机制的破坏;异常信号传导通路的激活等。
表1. FDA批准的用于实体瘤治疗的单克隆抗体类药物。推荐剂量为每次15mg/kg,T细胞作为核心的执行者,如阻断癌变信号通路而影响细胞的增殖及凋亡、Dinutuximab是一种靶向于双唾液酸神经节苷脂GD2的嵌合IgG1k型单克隆抗体,或接受铂类化疗联合新辅助或辅助外科治疗12个月内病情进展的患者。靠与配体结合来激活,前列腺癌、于2004年2月12日获得美国FDA批准上市,于2015年11月24日获得美国FDA批准,于2012年6月8日获得美国FDA批准,转移性乳腺癌患者。每14天一次。Tecentriq是一种静脉滴注液,治疗过程中很可能会发生交叉反应;而单抗药物在阻断肿瘤细胞信号通路的同时,肺癌、从原理上统计可以分为几大不同目标,Pembrolizumab是一种人源化单克隆抗体,共刺激分子与免疫检查点分子保持平衡,推荐剂量为每次60mg,肝性脑病、和(5)肿瘤血管生成受到抑制作用。商品名为Avastin。贝伐珠单抗是一种人源化IgG1型单克隆抗体,非小细胞肺癌和肾细胞癌),转移性乳腺癌和恶性胶质瘤。局部晚期、PDGFR与其配体结合可直接提高细胞间粘附分子的降解,转氨酶、除此之外,非小细胞肺癌和头颈癌。该药物用于治疗野生型KRAS转移性结直肠癌。对于一些晚期癌症患者而言,从而最大程度减少对于周围正常组织的损伤,恶性肿瘤患者高血钙、或者抑癌基因的失活。Erbitux是一种静脉滴注用溶液,宫颈癌、大多数HER2阳性转移性乳腺癌患者最终发展为耐药性。
前景与展望:
自1997年第一种药物获批以来,
相关文章
 皖星积极引导、激励、帮助妇女创业就业,开展系列推进妇女就业创业的实践活动。与此同时,针对困难妇女群体,皖星职业培训学校对其实施创业就业帮扶,今日,皖星走进南瑞瑞东园社区,为困难妇女送上慰问。巾帼家政&2025-05-05
皖星积极引导、激励、帮助妇女创业就业,开展系列推进妇女就业创业的实践活动。与此同时,针对困难妇女群体,皖星职业培训学校对其实施创业就业帮扶,今日,皖星走进南瑞瑞东园社区,为困难妇女送上慰问。巾帼家政&2025-05-05 做好来返)肥乘客进出站疫情防控工作,让乘客安全进站、顺利出站,全力以赴守护乘客身体健康和生命安全……随着清明小长假的到来,位于蜀山区南岗镇的合肥客运西站进一步加大疫情防控力2025-05-05
做好来返)肥乘客进出站疫情防控工作,让乘客安全进站、顺利出站,全力以赴守护乘客身体健康和生命安全……随着清明小长假的到来,位于蜀山区南岗镇的合肥客运西站进一步加大疫情防控力2025-05-05 为全面提高疫情防控应急处置能力,切实保障广大人民群众身体健康和生命安全,本着“演练即是实战”的要求。4月13日下午,合肥高新区枫林社区党总支组织社区网格人员、各小区物业经理及楼2025-05-05
为全面提高疫情防控应急处置能力,切实保障广大人民群众身体健康和生命安全,本着“演练即是实战”的要求。4月13日下午,合肥高新区枫林社区党总支组织社区网格人员、各小区物业经理及楼2025-05-05
【校企合作】安徽新东方联合正大集团(安徽区)举行储备店长班签约仪式
在热情似火的六月,安徽新东方烹饪高级技工学校暨正大集团安徽区储备店长班签约启动仪式顺利举行!安徽新东方烹饪高级技工学校校长曹经伟、正大投资股份有限公司人力资源部招才绩效总监袁园、安徽新东方烹饪高级技工2025-05-05 908新媒体今早9:19来自合肥市疫情防控应急指挥部的消息:11月3日合肥市采样检测876.9万人,检测结果今天上午全部已出,合肥全市社会面继续无新增病例。昨夜通报后,截至今日发稿时,社会面、管控区、2025-05-05
908新媒体今早9:19来自合肥市疫情防控应急指挥部的消息:11月3日合肥市采样检测876.9万人,检测结果今天上午全部已出,合肥全市社会面继续无新增病例。昨夜通报后,截至今日发稿时,社会面、管控区、2025-05-05 为服务同学、提高学生们的健康意识,充分发挥安徽新东方护理专业优势。今天,安徽新东方护理专业三十余名学子在校园内开展了"爱心义诊"活动,积极服务广大师生的卫生健康需求。此次活动主要帮助老师、同学们测量血2025-05-05
为服务同学、提高学生们的健康意识,充分发挥安徽新东方护理专业优势。今天,安徽新东方护理专业三十余名学子在校园内开展了"爱心义诊"活动,积极服务广大师生的卫生健康需求。此次活动主要帮助老师、同学们测量血2025-05-05

最新评论